中外製薬株式会社は5月8日、患者さんの臨床試験へのアクセス向上を目指し、新しい分散化臨床試験(decentralized clinical trial:DCT)の実施体制を導入し、進行固形がん患者さんを対象とした第1相臨床試験を開始したことを発表した。
同試験には、治験実施施設として国立がん研究センター中央病院が、またサテライト医療機関としてDCTによる負担軽減効果が期待できる地域(国立がん研究センター中央病院への移動時間が片道120分を超える地域)にある大阪医科薬科大学病院が参加。従来は治験実施施設で行っていた検査や評価の一部を、オンライン診療を活用したサテライト医療機関で実施する。また、オンライン診療にはMICINが提供するDCTプラットフォーム「MiROHA(ミロハ)」が使われており、eConsentを活用した遠隔再同意も実施予定だ。
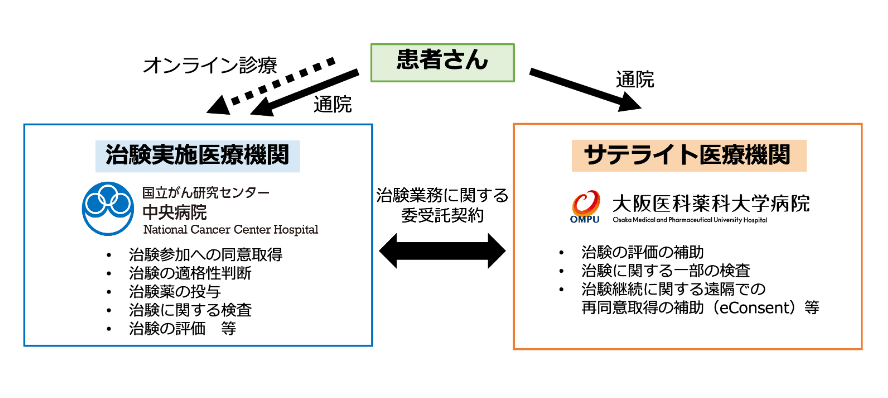
新薬候補の臨床試験は、限られた医療機関で行われるため、治験実施医療機関から離れたところに住む患者さんの通院に伴う時間的・経済的負担が問題である。実際、国立がん研究センター中央病院による研究でも、移動時間が片道120分を超えると、臨床試験への参加率が減少傾向にあることが明らかとなっており、患者さんが臨床試験にアクセスしやすい環境整備は、製薬会社・アカデミアをはじめ、臨床開発における共通の課題だ。
がんに対する企業主導の第1相臨床試験でのサテライト医療機関の活用への取り組みは、同試験が国内で初めて。DCTにおける新たな実施体制を評価し、居住地を問わず多くの患者さんが臨床試験にアクセスできる実施体制の構築が期待される。
参照元:
中外製薬 プレスリリース
この記事に利益相反はありません。