目次
- 1大腸がんと血管新生阻害剤アバスチン、サイラムザ、ザルトラップ
- 2肺がんと血管新生阻害剤アバスチン、サイラムザ
- 3胃がんと血管新生阻害剤サイラムザ
- 4血管新生阻害剤の違いとは
- 4-1
- 5ラムシルマブ(サイラムザ)の薬剤概要
- 5-1
- 5-2
- 5-3
- 5-4
- 5-5
- 5-6
- 5-7
- 6アフリベルセプト(ザルトラップ)の薬剤概要
- 6-1
- 6-2
- 6-3
- 6-4
- 6-5
- 6-6
- 6-7
- 6-8
- 6-9
 そこで本記事では国内に3製品も存在する血管新生阻害剤(VEGF阻害剤)の違いについて、有効性が確認された臨床試験の結果に基づき、がんの種類、治療ライン(1次/2次/3次以降)、併用薬の有無、患者背景などの要素に分けて紹介する。
本来ならば、血管新生阻害剤(抗VEGF阻害剤)同士で直接比較した臨床試験が存在すればその違いは簡単に分かるのだが、残念ながらそのような臨床試験は現在のところ存在しない。
そのため、血管新生阻害剤(抗VEGF阻害剤)の違いを本当の意味では理解できないが、少なくとも試験デザインが酷似した臨床試験の結果を比較することである程度の違いが見えてくるであろう。
なお、有効性が確認されているとは2017年11月13日現在で血管新生阻害剤(抗VEGF阻害剤)を開発した企業が主導する第III相試験における主要評価項目の結果が公表されていることと定義する。
そこで本記事では国内に3製品も存在する血管新生阻害剤(VEGF阻害剤)の違いについて、有効性が確認された臨床試験の結果に基づき、がんの種類、治療ライン(1次/2次/3次以降)、併用薬の有無、患者背景などの要素に分けて紹介する。
本来ならば、血管新生阻害剤(抗VEGF阻害剤)同士で直接比較した臨床試験が存在すればその違いは簡単に分かるのだが、残念ながらそのような臨床試験は現在のところ存在しない。
そのため、血管新生阻害剤(抗VEGF阻害剤)の違いを本当の意味では理解できないが、少なくとも試験デザインが酷似した臨床試験の結果を比較することである程度の違いが見えてくるであろう。
なお、有効性が確認されているとは2017年11月13日現在で血管新生阻害剤(抗VEGF阻害剤)を開発した企業が主導する第III相試験における主要評価項目の結果が公表されていることと定義する。
大腸がんと血管新生阻害剤アバスチン、サイラムザ、ザルトラップ
大腸がんに対する血管新生阻害剤(VEGF阻害剤)の第III相臨床試験は、アバスチン、サイラムザ、ザルトラップの3剤すべてにある。そのため、大腸がんにおける血管新生阻害剤(VEGF阻害剤)の違いを理解するためには3剤すべての第III相臨床試験の違いを理解しなければならない。 上記表は、大腸がんに対する血管新生阻害剤(VEGF阻害剤)3剤の第III相臨床試験の一覧である。ご覧の通り、各血管新生阻害剤(VEGF阻害剤)の有効性を証明した第III相臨床試験の本数はサイラムザ、ザルトラップが1本しかないのに対してアバスチンは複数本ある。
さらに、サイラムザ、ザルトラップの第III相臨床試験は治療ラインが2次治療、併用薬がFOLFIRI療法であるが、アバスチンはこれらと同等の第III相臨床試験を実施し、2次治療におけるFOFIRI併用療法での有効性を証明している。
つまり、サイラムザ、ザルトラップにあってアバスチンにない第III相臨床試験のエビデンスは現在のところ存在しないのだ。反対に、アバスチンにあってサイラムザ、ザルトラップにない第III相臨床試験はといえば、一次治療におけるFOLFOX/XELOX/SOX併用療法、FOLFIRI/IRIS/SIR併用療法、FOLFOXIRI併用療法、二次治療におけるFOLFOX/XELOX療法など複数ある。
以上のことから、大腸がんに対する血管新生阻害剤(VEGF阻害剤)の違いはアバスチンがサイラムザ、ザルトラップに比べて有効性を証明した第III相臨床試験の数が多いため、どの治療ラインどの併用薬でも組み合わせて使いやすい血管新生阻害剤(抗VEGF阻害剤)であるということである。
上記表は、大腸がんに対する血管新生阻害剤(VEGF阻害剤)3剤の第III相臨床試験の一覧である。ご覧の通り、各血管新生阻害剤(VEGF阻害剤)の有効性を証明した第III相臨床試験の本数はサイラムザ、ザルトラップが1本しかないのに対してアバスチンは複数本ある。
さらに、サイラムザ、ザルトラップの第III相臨床試験は治療ラインが2次治療、併用薬がFOLFIRI療法であるが、アバスチンはこれらと同等の第III相臨床試験を実施し、2次治療におけるFOFIRI併用療法での有効性を証明している。
つまり、サイラムザ、ザルトラップにあってアバスチンにない第III相臨床試験のエビデンスは現在のところ存在しないのだ。反対に、アバスチンにあってサイラムザ、ザルトラップにない第III相臨床試験はといえば、一次治療におけるFOLFOX/XELOX/SOX併用療法、FOLFIRI/IRIS/SIR併用療法、FOLFOXIRI併用療法、二次治療におけるFOLFOX/XELOX療法など複数ある。
以上のことから、大腸がんに対する血管新生阻害剤(VEGF阻害剤)の違いはアバスチンがサイラムザ、ザルトラップに比べて有効性を証明した第III相臨床試験の数が多いため、どの治療ラインどの併用薬でも組み合わせて使いやすい血管新生阻害剤(抗VEGF阻害剤)であるということである。
肺がんと血管新生阻害剤アバスチン、サイラムザ
肺がんに対する血管新生阻害剤(VEGF阻害剤)の第III相臨床試験は、アバスチン、サイラムザの2剤にあり、ザルトラップにはない。そのため、肺がんにおける血管新生阻害剤(VEGF阻害剤)の違いを理解するためには、アバスチンとサイラムザの第III相臨床試験の違いを理解しなければならない。 上記表は、肺がんに対する血管新生阻害剤(抗VEGF阻害剤)2剤の第III相臨床試験の一覧である。ご覧の通り、各血管新生阻害剤(抗VEGF阻害剤)の有効性を証明した第III相臨床試験の本数はサイラムザが1本しかないのに対してアバスチンは複数本ある。
そして、サイラムザが非小細胞肺がんの二次治療としてドセタキセル併用療法の有効性を証明した第III相臨床試験しかないのに対して、アバスチンは非小細胞肺がんの一次治療、二次治療、維持療法など複数の治療ラインで、ペメトレキセド(商品名アリムタ)、エルロチニブ(商品名タルセバ)、シスプラチン、カルボプラチンなどプラチナ系抗がん剤、ドセタキセル、パクリタキセルなどタキサン系抗がん剤など、複数の併用療法での有効性を証明した第III相臨床試験がある。
以上のことから、肺がんに対する血管新生阻害剤(VEGF阻害剤)の違いはアバスチンがサイラムザに比べて有効性を証明した第III相臨床試験の数が多いため、どの治療ラインどの併用薬でも組み合わせて使いやすい血管新生阻害剤(VEGF阻害剤)であるということである。
参考:【特集記事】非小細胞肺がん治療における血管新生阻害薬の現状と今後~近畿大学医学部内科学腫瘍内科部門教授 中川 和彦先生~(2017.02.17)
上記表は、肺がんに対する血管新生阻害剤(抗VEGF阻害剤)2剤の第III相臨床試験の一覧である。ご覧の通り、各血管新生阻害剤(抗VEGF阻害剤)の有効性を証明した第III相臨床試験の本数はサイラムザが1本しかないのに対してアバスチンは複数本ある。
そして、サイラムザが非小細胞肺がんの二次治療としてドセタキセル併用療法の有効性を証明した第III相臨床試験しかないのに対して、アバスチンは非小細胞肺がんの一次治療、二次治療、維持療法など複数の治療ラインで、ペメトレキセド(商品名アリムタ)、エルロチニブ(商品名タルセバ)、シスプラチン、カルボプラチンなどプラチナ系抗がん剤、ドセタキセル、パクリタキセルなどタキサン系抗がん剤など、複数の併用療法での有効性を証明した第III相臨床試験がある。
以上のことから、肺がんに対する血管新生阻害剤(VEGF阻害剤)の違いはアバスチンがサイラムザに比べて有効性を証明した第III相臨床試験の数が多いため、どの治療ラインどの併用薬でも組み合わせて使いやすい血管新生阻害剤(VEGF阻害剤)であるということである。
参考:【特集記事】非小細胞肺がん治療における血管新生阻害薬の現状と今後~近畿大学医学部内科学腫瘍内科部門教授 中川 和彦先生~(2017.02.17)
胃がんと血管新生阻害剤サイラムザ
胃がんに対する血管新生阻害剤(VEGF阻害剤)の第III相臨床試験はサイラムザの1剤しかない。そのため、胃がんにおける血管新生阻害剤(VEGF阻害剤)の違いはアバスチン、ザルトラップが胃がんに対して適応がなくサイラムザのみ適応があるという点である。 上記表は、胃がんに対する血管新生阻害剤(VEGF阻害剤)の第III相臨床試験の一覧である。血管新生阻害剤(VEGF阻害剤)として唯一胃がんに対する有効性を証明しているサイラムザは、ステージIV胃がんに対する2次治療としてパクリタキセル併用療法、または単剤療法でその有効性を証明している。
特にステージIV胃がん患者に対する2次治療としてのサイラムザ+パクリタキセル併用療法は、パクリタキセル単剤療法に対して主要評価項目である全生存期間を有意に延長(ハザード比0.807,95%信頼区間:0.678~0.962,p=0.0169)すること証明した結果、ステージIV胃がんに対する2次治療の標準治療となった。
上記表は、胃がんに対する血管新生阻害剤(VEGF阻害剤)の第III相臨床試験の一覧である。血管新生阻害剤(VEGF阻害剤)として唯一胃がんに対する有効性を証明しているサイラムザは、ステージIV胃がんに対する2次治療としてパクリタキセル併用療法、または単剤療法でその有効性を証明している。
特にステージIV胃がん患者に対する2次治療としてのサイラムザ+パクリタキセル併用療法は、パクリタキセル単剤療法に対して主要評価項目である全生存期間を有意に延長(ハザード比0.807,95%信頼区間:0.678~0.962,p=0.0169)すること証明した結果、ステージIV胃がんに対する2次治療の標準治療となった。
血管新生阻害剤の違いとは
以上のように、同じ作用機序を持つ血管新生阻害剤(VEGF阻害剤)でも、がんの種類を中心に、がんの進行具合(ステージIII/Ⅳ)、治療ライン(1次/2次/3次以降)、併用薬の有無、患者背景などの要素に分けてその違いを見ていくと、2017年10月29日現在でいくつかの違いが見つかる。 現在進行中の第III相臨床試験の本数が複数あることを考えると、この先いくつもの違いが血管新生阻害剤(抗EGF阻害剤)の間で見つかるに違いない。この違いが、血管新生阻害剤(抗VEGF阻害剤)の作用機序により生じた違いなのか?臨床試験のデザインにより生じた違いなのか?その真因は血管新生阻害剤(抗VEGF阻害剤)同士の直接比較試験を実施しない限りは明らかにならない。 しかし、その臨床試験の結果を待っていては何十年か先、下手すれば何十年経ってもその結果が出ない可能性は十二分にあり得る。そのため、科学的根拠レベルの信頼度が高いとされる第III相臨床試験を参考に、臨床試験のデザインが酷似した血管新生阻害剤(VEGF阻害剤)同士を比較することで何かしらの違いを見出すことは臨床的意義があると言えるだろう。3剤の薬価の比較
薬価は、アバスチン(400mg)が158,942円、サイラムザ(500mg)が355,450円、ザルトラップ(200㎎)が153,409円となる。 それぞれの大腸がんに対する1回の使用が、アバスチンが5mg/kg又は10mg/kg、サイラムザが1回8mg/kg、ザルトラップが1回4mg/kgとなっているため、体重60㎏の方が1回使用するのは以下のとおり。(*使用頻度はいずれの薬剤も2週に1回のことが多い) アバスチン(体重60kg×容量5mg/kg=300mg):158,942円×0.6=95,365.2円 サイラムザ(体重60kg×容量8mg/kg×=480mg):355,450円×0.96=341,232円 ザルトラップ(体重60kg×容量4mg/kg=125mg):153,409円×1.05=161,079.5円 よって、アバスチンが最も安く、ザルトラップ、サイラムザとなる。ラムシルマブ(サイラムザ)の薬剤概要
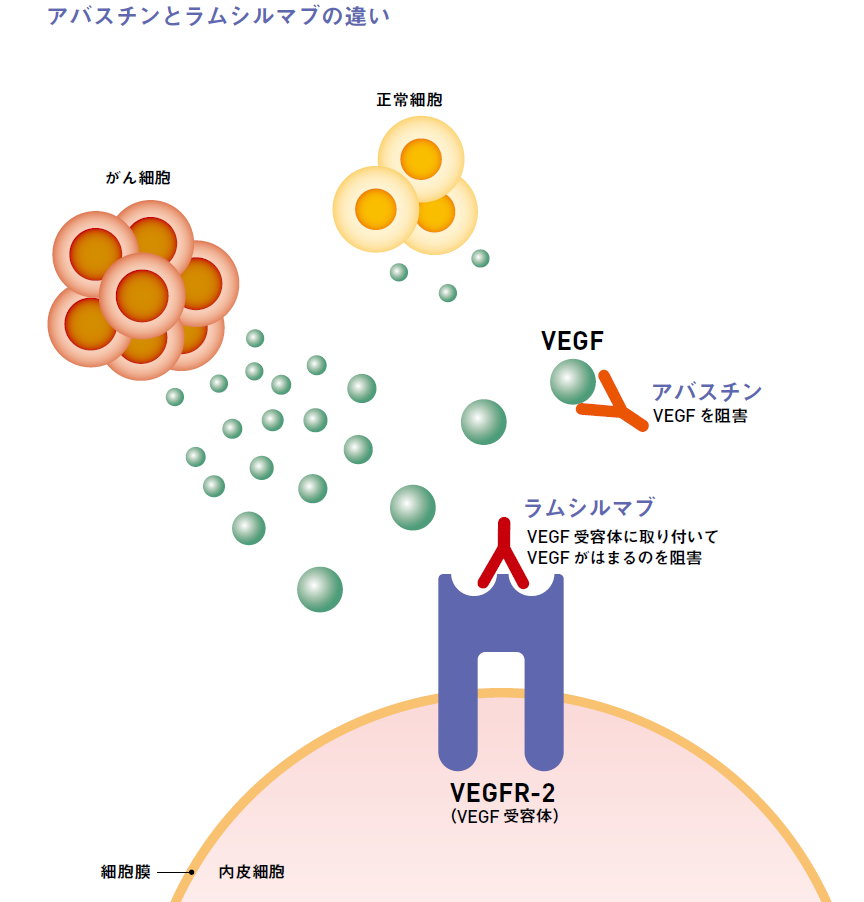
ラムシルマブ(サイラムザ)の作用機序
ロハス・メディカル
ラムシルマブ(サイラムザ)はヒトVEGFR-2に対する特異的な抗体であり、VEGFリガンド(VEGF-A、VEGF-C、VEGF-D)のVEGFR-2への結合を阻害することで、VEGFR-2の活性化を阻害し、内皮細胞の増殖、遊走及び生存を阻害し、腫瘍血管新生を阻害します。製品名
サイラムザ一般名
ラムシルマブ(ramucirumab)用法用量
1. 治癒切除不能な進行・再発の胃癌 通常、成人には2週間に1回、ラムシルマブ(遺伝子組換え) と して1回8mg/kg(体重)をおよそ60分かけて点滴静注する。 なお、患者の状態により適宜減量する。 2. 治癒切除不能な進行・再発の結腸・直腸癌 イリノテカン塩酸塩水和物、レボホリナート及びフルオロ ウラシルとの併用において、通常、成人には2週間に1回、ラムシルマブ(遺伝子組換え)として1回8mg/kg(体重)をおよ そ60分かけて点滴静注する。なお、患者の状態により適宜減量する。 3. 切除不能な進行・再発の非小細胞肺癌 ドセタキセルとの併用において、通常、成人には3週間に1 回、ラムシルマブ(遺伝子組換え)として1回10mg/kg(体重) をおよそ60分かけて点滴静注する。なお、患者の状態により 適宜減量する。効能効果
治癒切除不能な進行・再発の胃癌、治癒切除不能な進行・再発の結腸・直腸癌、切除不能な進行・再発の非小細胞肺癌主な副作用
好中球減少症、鼻出血、口内炎、血小板減少症、高血圧製造承認日
2015年6月(治癒切除不能な進行・再発の胃癌)アフリベルセプト(ザルトラップ)の薬剤概要
アフリベルセプト(ザルトラップ)の作用機序
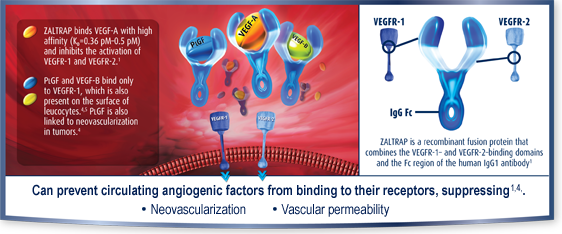 アフリベルセプト(ザルトラップ)はヒトVEGF受容体 1及び2の細胞外ドメインをヒトIgG1のFcドメインに結合した組換え融合糖蛋白質であり、可溶性のデコイ受容体として血管内皮細胞増殖因子A(VEGF-A)、VEGF-B、胎盤増殖因子(PIGF)に結合する可溶性受容体として、本来の受容体よりも高い親和性で結合することにより、血管新生と血管透過性を抑制し抗腫瘍効果を発揮する。
アフリベルセプト(ザルトラップ)はヒトVEGF受容体 1及び2の細胞外ドメインをヒトIgG1のFcドメインに結合した組換え融合糖蛋白質であり、可溶性のデコイ受容体として血管内皮細胞増殖因子A(VEGF-A)、VEGF-B、胎盤増殖因子(PIGF)に結合する可溶性受容体として、本来の受容体よりも高い親和性で結合することにより、血管新生と血管透過性を抑制し抗腫瘍効果を発揮する。





 オンコロとは
オンコロとは
 メディカル・サポーター
メディカル・サポーター
 Remember Girl’s Power!!
Remember Girl’s Power!!
 0120-974-268
0120-974-268