国立がん研究センター、大阪国際がんセンター、および九州大学病院は3月2日、一次治療の効果が得られなくなった進行期小腸腺がんの患者を対象に、抗体薬物複合体(ADC)であるエンホルツマブ ベドチン(製品名:パドセブ)の有効性および安全性を評価する
多施設共同単群第II相医師主導治験(ENVELOPE試験/NCCH2412試験)を開始したと発表した。小腸腺がんに対してADCを用いた治験は、世界に先駆けた取り組みとなる。
小腸腺がんは全悪性腫瘍のうちの0.5%以下を占める極めて稀な希少がんである。初期段階では症状が現れにくく、診断時にはすでに進行していることが多い。現在、外科的切除が困難な進行期の小腸腺がんに対する一次治療としては、FOLFOX療法などの全身化学療法が用いられているが、効果持続期間の中央値は約6か月にとどまる。さらに、一次治療が無効または継続困難となった後に使用できる既承認薬はなく、二次治療は確立されていないため、新たな治療選択肢の開発が大きな課題となっている。
こうした背景の中、国立がん研究センター中央病院の研究チームは、新たな治療選択肢としてがん細胞を選択的に攻撃するADCに着目。探索の結果、尿路上皮がんの治療薬としてすでに承認されているエンホルツマブ ベドチンの標的腫瘍抗原である「ネクチン-4(Nectin-4)」が、小腸腺がんにおいても約82%という高頻度で発現していることを発見した。この発現頻度は尿路上皮がんでの発現率と同程度であり、エンホルツマブ ベドチンが小腸腺がんにも効果を示す可能性が示唆されたため、同治験が立ち上げられた。
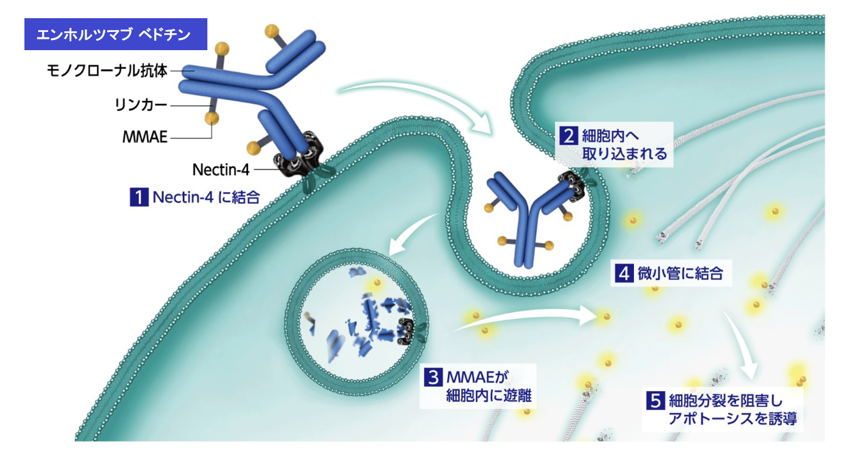
(画像はリリースより)
ENVELOPE試験の主な対象となるのは、以下の条件などを満たす患者である。
- 試験参加について、患者さんご本人から文書による同意が得られる
- 治験への登録時において、年齢が18歳以上
- 手術により切除ができない、または小腸周辺以外に広がっている小腸腺がんと診断されている
- FOLFOX療法またはCapeOX療法のいずれかの抗がん剤治療を受け、効果がなくなった、または副作用で中止になった
- 遺伝子パネル検査などの結果によって推奨されている分子標的治療薬や免疫療法薬が無効、あるいは副作用で継続できない、あるいは合併症などで実施困難
- 各臓器機能が規定内に保たれている
投与スケジュールは、28日を1コースとし、エンホルツマブ ベドチンを週1回、3週間連続で点滴投与した後、4週目を休薬とする。効果がなくなるか副作用で継続困難になるまで投与を継続する。目標登録人数は合計27人で、国立がん研究センター中央病院、大阪国際がんセンター、九州大学病院の3施設で実施される。
同治験によってエンホルツマブ ベドチンの有効性が示された場合、進行性または転移性の小腸腺がんに対する新たな治療薬としての薬事承認を目指すという。また、小腸腺がんの二次治療は欧米を含む国際的にも確立されていないため、同試験の成果が米国の治療ガイドラインなど海外の診療指針に反映される可能性もあり、国際共同研究グループとの連携による治療開発も視野に入れている。
参照元:
国立がん研究センター プレスリリース
 (画像はリリースより)
ENVELOPE試験の主な対象となるのは、以下の条件などを満たす患者である。
(画像はリリースより)
ENVELOPE試験の主な対象となるのは、以下の条件などを満たす患者である。





 オンコロとは
オンコロとは
 メディカル・サポーター
メディカル・サポーター
 Remember Girl’s Power!!
Remember Girl’s Power!!
 0120-974-268
0120-974-268